LA NATURALEZA BÁSICA DE LA VIDA
BIOLOGÍA Y GEOLOGÍA
8. PROTEÍNAS
Son biomoléculas orgánicas formadas por C, O, H, N, [S]. Son biopolímeros formados por la unión de subunidades llamadas aminoácidos.AMINOÁCIDOS (aa)
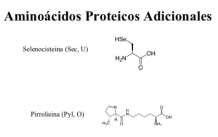
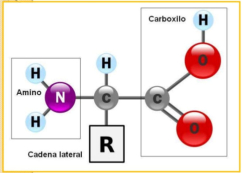
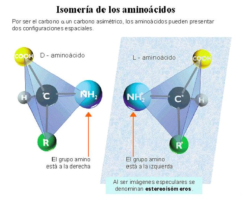
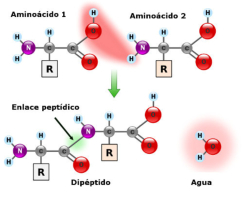
Son moléculas formadas por un C central (Cα) unido a un grupo amino (-NH2), un grupo ácido o carboxilo (- COOH), un átomo de H y una cadena lateral variable (R). Existen 20 aa en las proteínas de los seres vivos (aa proteicos), aunque hay otros muchos (más de 200). La diferencia entre ellos está en la cadena R. Los aa presentan isomerías. Entre otras, pueden ser D o L. Todos los aa proteicos son L. Los D aparecen en bacterias y en algunos antibióticos. Los aa se unen entre sí mediante enlaces peptídicos. Este enlace consiste en la unión del grupo carboxilo de un aa con el grupo amino de otro, liberando una molécula de agua. La unión de 2 aa forma un dipéptido (existen 20 2 posibles); 3, tripéptidos (20 3 ) y, en general, polipéptidos (20 n ).PROTEÍNAS
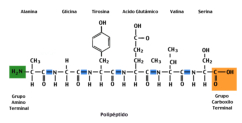
Una proteína es una molécula formada por una o varias cadenas polipeptídicas (incluso de miles de aa). Las proteínas se diferencian por el número, tipo y secuencia de aa de sus cadenas. Toda proteína tiene un extremo amino libre (N terminal o amino terminal) y un extremo carboxilo libre (C terminal). Por convenio, se considera que las cadenas empiezan por el extremo N terminal y acaban en el C terminal.Estructura de las proteínas
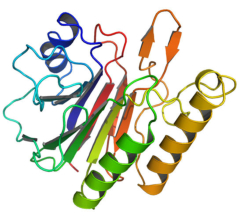
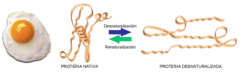
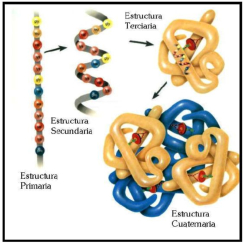
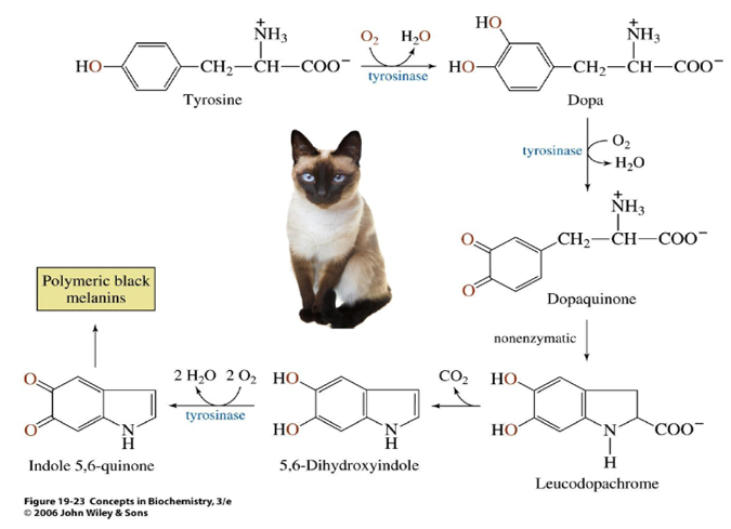
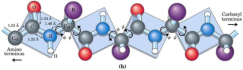
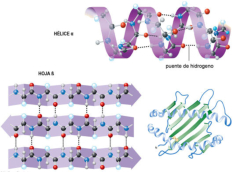
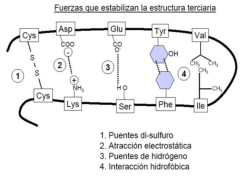
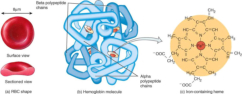
Las propiedades más importantes de las proteínas derivan de su estructura tridimensional. Ésta tiene varios niveles de complejidad, cada uno de los cuales deriva del anterior. 1. Estructura primaria: es la secuencia de aa de la cadena polipeptídica. Los polipéptidos no pueden girar alrededor del enlace peptídico, lo que hace que los átomos del mismo estén en un mismo plano. Así, la cadena polipeptídica se asemeja a una sucesión de placas planas articuladas. 2. Estructura 2 ria : es el plegamiento espontáneo de la cadena polipeptídica en el espacio. Puede ser α-hélice y β-laminar. La mayoría de las proteínas tienen zonas con ambas estructuras. 3. Estructura 3 ria : configuración espacial final de la proteína, con una estructura, en general, globular. La estructura se mantiene por enlaces débiles: puentes de H, fuerzas electrostáticas, fuerzas de Van der Waals y, en algunos casos, puentes disulfuro. 4. Estructura 4 ria : es la que aparece en proteínas formadas por varias cadenas polipeptídicas unidas entre sí. Dímeros (citocromo C); tetrámeros (hemoglobina); polímeros (actina y miosina, ribosomas, cápsida de virus). La unión entre cadenas se da por los mismos enlaces que en la terciaria. La estructura de las proteínas determina su función. Los cambios extremos del medio (temperatura, pH, presión, electricidad, presencia de iones), pueden hacerles perder la estructura tridimensional: desnaturalización: Las proteínas se convierten en filamentos fibrosos insolubles (huevo cocido, melanina en el gato siamés). La desnaturalización puede ser reversible (renaturalización) o irreversible (clara de huevo cocido). Al desnaturalizarse dejan de ser solubles, precipitan y pierden su funcionalidad.Funciones de las proteínas
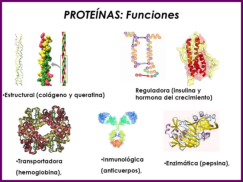
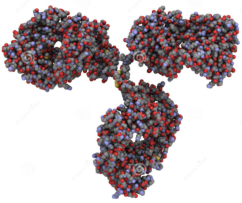
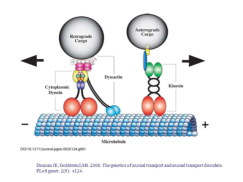
Los seres vivos tienen miles de proteínas diferentes (algunas exclusivas), cada una con una determinada función, por lo que las proteínas son las moléculas con más funciones: Estructural: colágeno (tendones, huesos, cartílagos); queratina (epidermis, escamas, uñas, pelo, plumas); fibroína (tela de araña y orugas), … Transportadora: hemoglobina (oxígeno en vertebrados); hemocianina (en invertebrados); lipoproteínas (colesterol). Hormonal (reguladora): insulina y glucagón (controlan el metabolismo de los glúcidos); hormona del crecimiento; … Contráctil: dineína (cilios y flagelos); actina y miosina (fibras musculares); … Defensa: trombina y fibrinógeno (coagulación sanguínea); mucina (germicida de mucosas); inmunoglobulinas (anticuerpos: defensa inmunitaria); … Reserva energética: ovoalbúmina (clara de huevo); caseína (leche); … Homeostática: regulan el equilibrio osmótico y el pH (como ácidos y como bases). Enzimática o biocatalizadora: quizá la función más importante. Catalizan todas las reacciones metabólicas de los seres vivos: enzimas.9. ENZIMAS
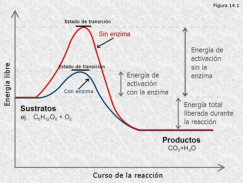
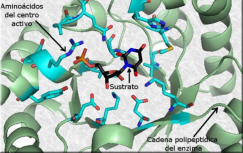
Son proteínas que actúan como catalizadores biológicos, aumentando la velocidad de las reacciones metabólicas. Las enzimas son altamente específicas de las reacciones que catalizan. Ello se debe a su estructura tridimensional, en la cual existe una región denominada centro activo o catalítico, que se adapta perfectamente a la molécula a la que se unen.MECANISMO DE ACCIÓN ENZIMÁTICA
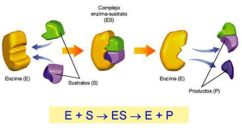
Las enzimas actúan uniéndose de forma temporal a un reactivo específico llamado sustrato. La unión se realiza en el centro activo y es específica para cada sustrato. Se forma así un complejo enzima-sustrato. Esta unión no es fuerte, pero la enzima crea un entorno apropiado para que el sustrato cambie y se convierta en el producto o productos de la reacción. Tras la reacción, la enzima se libera intacta y puede volver a actuar sobre otro sustrato. Las enzimas se clasifican por la reacción que catalizan: hidrolasas, ligasas, fosfatasas, oxidorreductasas,… Para nombrarlas se añade el sufijo –asa al nombre del sustrato que catalizan o del tipo de reacción: sacarasa, peptidasa, lipasa, proteasa, …PROPIEDADES DE LAS ENZIMAS
Como proteínas que son, tienen sus mismas propiedades y, además: Especificidad: una enzima sólo puede actuar sobre un sustrato o un grupo de ellos similares, y sólo catalizan un tipo de reacción. Eficiencia: las enzimas catalizan a una enorme velocidad, hasta miles de moléculas por segundo y, además, no se consumen en el proceso. Por ello se necesitan en pequeñas cantidades. Como en toda proteína, los cambios de pH, temperatura y otros pueden impedir o limitar su actuación (desnaturalización).

- Naturaleza básica de la vida
- Organización celular
- Organización pluricelular: animales
- Tejidos vegetales
- Diversidad: Moneras, Protoctistas, Hongos
- Diversidad: plantas y animales no cordados
- Diversidad: cordados
- Digestivo animal
- Circulatorio animal
- Respiratorio y excretor animal
- Reproductor animal
- Neuroendocrino
- Nutrición en plantas: fotosíntesis
- Otras formas de nutrición. Movimientos.
- Reproducción en plantas
- Historia de la Tierra
- Prácticas de laboratorio
- Vídeos
- Exámenes y trabajos
- Cálculo Nota Final






Para ir a donde no se sabe hay que ir por donde no se sabe.” San Juan de la Cruz
“It must be a strange world not being a scientist, going through life not knowing--or
maybe not caring about where the air came from, where the stars at night came from
or how far they are from us. I WANT TO KNOW” Michio Kaku
“Nullius in verba” Robert Boyle, Christopher Wren y Robert Hooke


- Naturaleza básica de la vida
- Organización celular
- Organización pluricelular: animales
- Tejidos vegetales
- Diversidad: Moneras, Protoctistas, Hongos
- Diversidad: plantas y animales
- Digestivo animal
- Circulatorio animal
- Respiratorio y excretor animal
- Reproductor animal
- Neuroendocrino
- Nutrición en plantas
- Otras formas de nutrición. Movimientos
- Reproducción en plantas
- Historia de la Tierra
- Prácticas de laboratorio
- Vídeos
- Exámenes y trabajos
- Cálculo Nota Final

Paganini: ¿síndrome de Marfan?