LA NATURALEZA BÁSICA DE LA VIDA
BIOLOGÍA Y GEOLOGÍA
3. AGUA
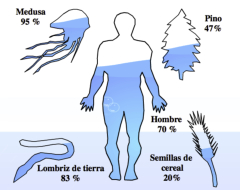
El agua es la molécula más abundante de la biosfera. Los seres vivos contienen entre el 65 y el 90% de agua. Además de formar parte de los organismos, con toda seguridad participó en las reacciones que condujeron a la aparición de la vida. Sin embargo a pesar de su abundancia, el agua no es una molécula corriente. Tiene sorprendentes propiedades que la hicieron idónea para la vida.LA MOLÉCULA DE AGUA
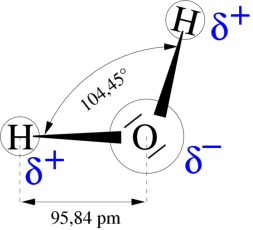
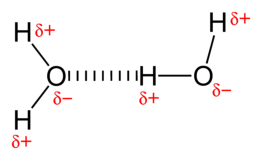
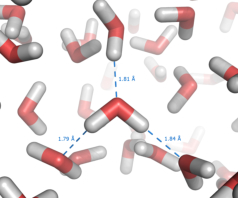
La molécula de agua está formada por dos átomos de H y uno de O. Pero la disposición tetraédrica de los orbitales del oxígeno determina un ángulo entre ambos H de 104,5º. Por otra parte, el O es más electronegativo que el H, por lo que atrae con más fuerza a los electrones. Como consecuencia, aunque la molécula de agua es neutra (tiene tantas cargas positivas como negativas), sus electrones están distribuidos de forma asimétrica, por lo que es una molécula polar: alrededor del O hay una densidad de carga negativa (δ-) y alrededor de los H una densidad de carga positiva (δ+). Debido a esta polaridad se establecen interacciones con otras moléculas polares y con iones cargados eléctricamente. Entre las propias moléculas de agua se establecen interacciones dipolo-dipolo, formando un tipo de enlaces llamados enlaces o puentes de H. Aunque estas uniones son débiles y sólo duran una fracción de segundo, su gran número (cada molécula de agua puede unirse a otras 4) le da al agua (líquida o sólida) una estructura reticular, responsable en buena parte de sus características peculiares.PROPIEDADES E IMPORTANCIA BIOLÓGICA DEL AGUA
Acción disolvente
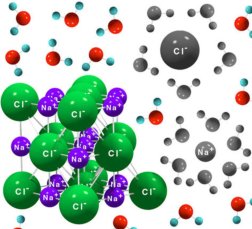
Es el líquido que más sustancias disuelve (disolvente universal). Forma puentes de hidrógeno con otras sustancias polares (grupos –OH de alcoholes y azúcares; -NH2 de aminoácidos, proteínas, ácidos nucleicos, etc) y las disuelve. El agua también disuelve compuestos iónicos, como sales, ya que los iones son atraídos por los dipolos del agua, que crea una capa de solvatación o hidratación alrededor de cada ion, debilitando su unión a la sal. La capacidad de disolución del agua es responsable de dos funciones biológicas: Es el medio donde se da la mayoría de reacciones metabólicas: las moléculas han de estar disueltas. Muchas propiedades de proteínas, ác. nucleicos y otras biomoléculas dependen de su interacción con el agua. El transporte de nutrientes y desechos se da en medio acuoso (sangre, linfa, savia) en forma de sustancias disueltas.Gran calor específico o capacidad térmica
El agua puede almacenar gran cantidad de energía a determinada temperatura. Almacena calor sin aumentar notablemente su temperatura y, al revés, se enfría más lentamente que otros líquidos al liberar energía. Esto se debe a los enlaces de H, que deben romperse o formarse cuando se calienta o enfría el agua. Funciones: El agua actúa como tampón térmico, manteniendo la temperatura con cierta independencia del medio (homeotermia). El calor de las reacciones químicas se difunde rápidamente, sin acumularse en puntos concretos.Elevado calor de vaporización
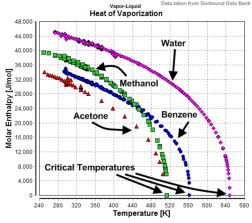
Debido a que han de romperse los puentes de hidrógeno, se precisa mucha energía para evaporar el agua. Por ello, al evaporarse, disminuye la temperatura. Funciones: Refrigeración: animales (sudor) y plantas (esencias volátiles de tomillo, romero…) utilizan esta propiedad para refrescarse cuando hace calor.Elevada fuerza de cohesión
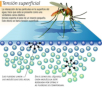
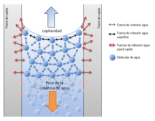
La cohesión es la fuerza que mantiene unidas a las moléculas de agua. El agua es incompresible debido a la estructura que forman sus puentes de hidrógeno. Funciones: Esqueleto hidrostático: el agua es el soporte de algunos animales, como gusanos perforadores, capaces de horadar la roca. Tensión superficial: permite soportar el peso de pequeños animales sobre la superficie.Elevada fuerza de adhesión
La adhesión es la fuerza que mantiene unidas a diferentes moléculas. También debida a los puentes de hidrógeno entre el agua y otras moléculas. Funciones: Responsable, junto a la cohesión, de la capilaridad, la capacidad del agua para ascender por tubos estrechos (transporte de la savia bruta).Menor densidad del hielo que del agua líquida
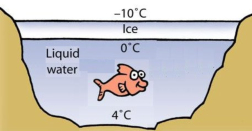
El agua permanece líquida entre 0 y 100 ºC. Además, alcanza su mayor densidad a los 4ºC. Así, el hielo es menos denso que el agua líquida y flota. Funciones: Supervivencia de especies en masas de agua congelada: aunque el agua superficial se congele, el interior permanece líquido y a unos 4-5 ºC.










- Naturaleza básica de la vida
- Organización celular
- Organización pluricelular: animales
- Tejidos vegetales
- Diversidad: Moneras, Protoctistas, Hongos
- Diversidad: plantas y animales no cordados
- Diversidad: cordados
- Digestivo animal
- Circulatorio animal
- Respiratorio y excretor animal
- Reproductor animal
- Neuroendocrino
- Nutrición en plantas: fotosíntesis
- Otras formas de nutrición. Movimientos.
- Reproducción en plantas
- Historia de la Tierra
- Prácticas de laboratorio
- Vídeos
- Exámenes y trabajos
- Cálculo Nota Final






Para ir a donde no se sabe hay que ir por donde no se sabe.” San Juan de la Cruz
“It must be a strange world not being a scientist, going through life not knowing--or
maybe not caring about where the air came from, where the stars at night came from
or how far they are from us. I WANT TO KNOW” Michio Kaku
“Nullius in verba” Robert Boyle, Christopher Wren y Robert Hooke




- Naturaleza básica de la vida
- Organización celular
- Organización pluricelular: animales
- Tejidos vegetales
- Diversidad: Moneras, Protoctistas, Hongos
- Diversidad: plantas y animales
- Digestivo animal
- Circulatorio animal
- Respiratorio y excretor animal
- Reproductor animal
- Neuroendocrino
- Nutrición en plantas
- Otras formas de nutrición. Movimientos
- Reproducción en plantas
- Historia de la Tierra
- Prácticas de laboratorio
- Vídeos
- Exámenes y trabajos
- Cálculo Nota Final

elmundotoday
Verificado
La nueva «agua H2O» de Font Vella
incorpora dos átomos de hidrógeno por
cada uno de oxígeno. «Según nuestros
análisis, el 60% del cuerpo humano está
hecho de Font Vella, lo que nos convierte
en un producto esencial para la vida»,
explican fuentes cercanas al departamento
de desarrollo de la firma.




Cuadro impresionista de Samantha French